泽璟制药:6月17日召开分析师会议,华夏基金、富国基金等多家机构参与
证券之星消息,2024年6月27日泽璟制药(688266)发布公告称公司于2024年6月17日召开分析师会议,华夏基金、富国基金、中海基金、中银基金、华安基金、国信资管、光大保德信、红骅投资、君阳基金、东方阿尔法基金、中邮基金、华宝基金、君弘资产、金鹰基金、财信证投、华西基金、安信基金、玄元投资、万和自营、人保养老、金鼎资本、远信投资、中金基金、中金资管、正心谷、东方自营、国君资管、趣时资本、淳厚基金、诺德基金、新华资产、前海开源、鹏华基金、长城基金、诺安基金、润晖基金参与。
具体内容如下:
问:请介绍一下吉卡昔替尼治疗斑秃的临床情况和研发进展?
答:《盐酸杰克替尼片治疗重症斑秃患者的有效性和安全性的多中心、随机、双盲、安慰剂平行对照 III 期临床试验》(方案编号ZGJK018)在北京大学人民医院、中国医学科学院皮肤病医院等44家医院开展,符合方案要求的425例重症斑秃患者随机入组,分配到吉卡昔替尼片50mg Bid 组、75mg Bid组或安慰剂片组,经独立第三方非盲团队对该项试验中完成 24周治疗的数据进行分析后,结果显示主要疗效终点,即治疗24周脱发严重程度工具量表(SLT)评分≤20分的受试者百分率,吉卡昔替尼片两组均显著优于安慰剂组,达到统计显著性(p<0.0001)。安全性方面,吉卡昔替尼治疗重症斑秃患者的安全性与耐受性良好。有关该项临床试验的详细数据,将在后续相关学术会议上公布。公司将加快推进盐酸吉卡昔替尼片治疗重症斑秃患者适应症的上市进程。
目前,吉卡昔替尼治疗重症斑秃III期临床研究的延伸试验(方案编号ZGJK020)正在进行中。问:重组人促甲状腺激素目前进展情况、市场展望?
答:公司已向国家药监局递交了注射用重组人促甲状腺激素(rhTSH)递交了生物制品上市许可申请,并于近日获得受理。本次受理新药上市申请的适应症是用于既往接受过甲状腺切除术的分化型甲状腺癌患者随访时的放射性碘(131I)全身显像(WBS)检查和血清甲状腺球蛋白(Tg)检测。截至目前,国内尚未有重组人促甲状腺激素获批用于该项适应症。
分化型甲状腺癌是甲状腺癌的主要亚型,约占甲状腺癌新发病例数的 90%。近年来,甲状腺癌的发病率呈持续上升趋势,根据国家癌症中心发布的2022年中国恶性肿瘤流行病权威数据,甲状腺癌2022年新发患者 46.61万人,仅次于肺癌及结直肠癌,为中国第三大高发的恶性肿瘤。由于中国分化型甲状腺癌新发病例数的增长所带来的复查监测与治疗的需求增加,未来分化型甲状腺癌术后诊断及术后治疗的市场空间有望不断扩大。问:请介绍一下重组人促甲状腺激素的应用场景?
答:注射用重组人促甲状腺激素(rhTSH)应用场景为对于甲状腺癌患者诊疗过程一般包括手术切除、I-131放疗、系统治疗等。分化型甲状腺全切或近全切手术后的诊疗,I-131治疗和定期随访是获得更长生存的关键手段之一。外源性注射人重组促甲状腺素是比现有甲状腺素撤除(THW)更加快速和安全地提高甲状腺癌诊断和治疗水平的方法。相较于现有的甲状腺素撤除(THW)方法(如停用优甲乐2~4周),注射重组人促甲状腺激素提升TSH时间更快(仅需2天左右),并且避免甲减导致体重增加、畏寒等不良反应以及相关并发症的恶化,降低肿瘤进展风险,因此是临床上甲状腺癌诊断和治疗的更优选择。
问:请公司ZG005在ASCO发布的临床研究数据情况和展望?
答:ZG005在2024年美国临床肿瘤学会(SCO)年会发布的I/II期临床研究数据及最新进展截至2024年4月16日,ZG005-001项目剂量递增阶段已完成,共入组32例受试者;剂量扩展阶段正在进行中,已入组47例受试者。79例受试者中,43%的受试者既往曾接受过至少两线抗肿瘤药物系统治疗,48%的受试者既往接受过PD-1/PD-L1抑制剂治疗。
有效性方面,可评估疗效的21例宫颈癌受试者(3 mg/kg组1例、10 mg/kg组12例、20 mg/kg组8例)中,有2例完全缓解(CR)、7例部分缓解(PR)和8例疾病稳定(SD);客观缓解率(ORR)为43%(9/21),疾病控制率(DCR)为81%(17/21),特别是目标剂量20 mg/kg组的客观缓解率(ORR)达到63%。9例获得客观缓解(CR/PRs)的宫颈癌受试者中,2例既往接受过PD-1/PD-L1抑制剂治疗。1例3 mg/kg组宫颈癌受试者,其肿瘤病灶自首次给药后持续缩小,现已接受ZG005治疗超过77周,靶病灶总径较基线缩小60.9%。11例宫颈癌受试者在首次肿瘤评估时即出现肿瘤缩小。截至数据截止日期,有16例受试者仍正在接受治疗。安全性方面,63.3%(50/79)的受试者出现了与治疗相关的不良事件(TREs),绝大多数严重程度为1或2级。综上,ZG005呈现出良好的耐受性和安全性及良好的抗肿瘤疗效,特别是在接受20 mg/kg剂量治疗的晚期宫颈癌患者中初步结果显示疗效更优。现有已获得的有效性和安全性数据支持ZG005在晚期宫颈癌等多瘤种中开展进一步的临床研究。根据公开查询,ZG005是全球率先进入临床研究的同靶点药物之一,目前全球范围内尚未有同类机制药物获批上市。问:请介绍ZG006的产品作用机制、研发进展和后续开发计划?
答:ZG006是全球第一个针对DLL3表达肿瘤的三特异性抗体(CD3×DLL3×DLL3),是全球同类首创(First-in-Class)分子形式,具有成为同类最佳(Best-in-Class)分子的潜力。目前全球只有安进公司的同靶点药物MG757(CD3/DLL3双抗)提交了美国FD上市申请,但还未有针对DLL3靶点的新药获批上市。ZG006衔接肿瘤细胞和T细胞,将T细胞拉近肿瘤细胞,从而利用T细胞特异性杀伤肿瘤细胞。ZG006用于治疗晚期实体瘤的临床试验申请已获FD和NMP批准,目前处于I期的剂量爬坡阶段,入组进度顺利,符合预期。
基于DLL3是一种在正常细胞中极低表达,而在小细胞肺癌(SCLC)、神经内分泌癌等肿瘤细胞中高表达的肿瘤特异性抗原,公司将重点在小细胞肺癌、神经内分泌癌等领域进行开发和研究。问:吉卡昔替尼在自身免疫性疾病领域的研发进展?
答:在自身免疫性疾病领域,吉卡昔替尼片治疗重症斑秃的III期临床研究已达到主要疗效终点,公司将加快推进盐酸吉卡昔替尼片治疗重症斑秃患者适应症的上市进程,该适应症的研发进度位于国产JK抑制剂的前列;同时,吉卡昔替尼片治疗中重度特应性皮炎和强直性脊柱炎的III期临床试验也在加快推进中,吉卡昔替尼片治疗特发性肺纤维化、中重度斑块状银屑病等自身免疫相关疾病的II期临床试验正在开展中。在治疗白癜风适应症方面,吉卡昔替尼乳膏和吉卡昔替尼片剂用于治疗12岁及以上青少年和成人非节段型白癜风患者的临床试验已经获得NMP批准。
问:吉卡昔替尼治疗中高危骨髓纤维化的审批进展,以及后续获批后商业化策略?
答:吉卡昔替尼片治疗中、高危骨髓纤维化适应症目前正处于新药上市申请审评进程中,公司正积极与药监部门开展沟通,以加快推进审评进程。
针对吉卡昔替尼片治疗骨髓纤维化适应症后续获批后的商业化工作,公司已在提前积极布局,公司将在现有商业化团队核心骨干架构的基础上,新增招聘擅长血液病领域的市场、医学和销售推广的优秀人才,进行吉卡昔替尼片获批后的市场推广和销售。公司将在吉卡昔替尼片获批后依托其显著的有效性和安全性优势,不断提升市场占有率,为国内骨髓纤维化患者带来新的治疗选择。问:请公司泛KRAS抑制剂ZG2001的特点和研发进展?
答:ZG2001是公司开发的一种新型的口服泛KRS突变抑制剂,属于1类新药,主要适应症是用于治疗KRS突变的肿瘤。ZG2001可特异性地与SOS1的催化区域结合,阻止其与失活状态KRS-GDP的相互作用并同时阻断SOS1驱动的反馈,减少KRS-GTP激活状态的形成,从而抑制MPK信号通路在KRS突变依赖性癌症中的作用,发挥抗肿瘤作用。经公开信息查询,目前全球还未有相同作用机制药物上市。
ZG2001片用于治疗KRS突变的晚期实体瘤的临床试验已经获得国家药品监督管理局(NMP)和美国食品药品监督管理局(FD)批准,公司正在国内开展I期临床试验,积极推进该新药的研发进程。泽璟制药(688266)主营业务:化学新药及生物新药的研发、生产及销售。
泽璟制药2024年一季报显示,公司主营收入1.08亿元,同比上升0.12%;归母净利润-3949.94万元,同比上升30.98%;扣非净利润-4250.29万元,同比上升33.51%;负债率48.44%,投资收益50.59万元,财务费用-696.08万元,毛利率93.4%。
该股最近90天内共有12家机构给出评级,买入评级11家,增持评级1家;过去90天内机构目标均价为63.04。
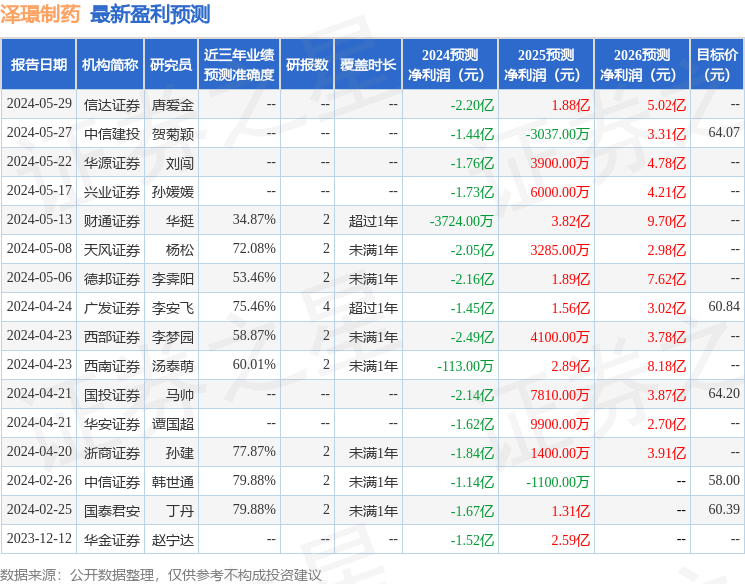
以下是详细的盈利预测信息:
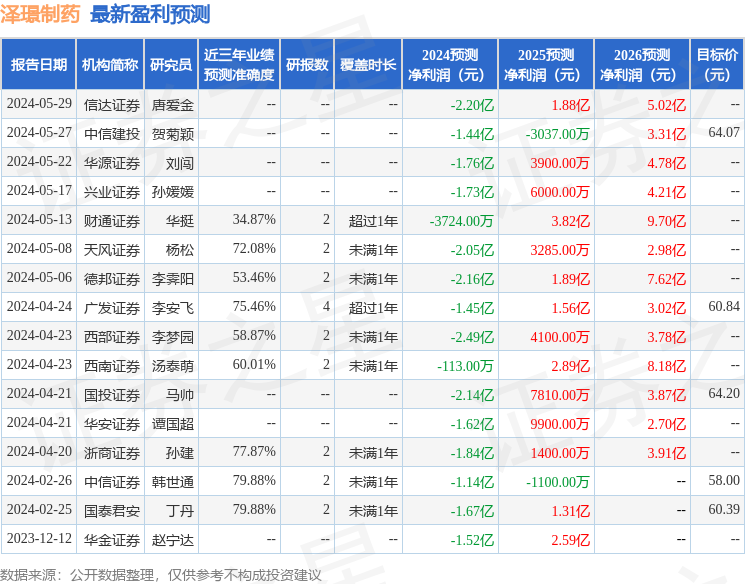
融资融券数据显示该股近3个月融资净流出972.65万,融资余额减少;融券净流出2125.56万,融券余额减少。
以上内容由证券之星根据公开信息整理,由算法生成(网信算备310104345710301240019号),与本站立场无关,如数据存在问题请联系我们。本文为数据整理,不对您构成任何投资建议,投资有风险,请谨慎决策。
交易商排行
更多- 监管中EXNESS10-15年 | 英国监管 | 塞浦路斯监管 | 南非监管93.02
- 监管中FXTM 富拓10-15年 |塞浦路斯监管 | 英国监管 | 毛里求斯监管88.21
- 监管中FXBTG10-15年 | 澳大利亚监管 |83.48
- 监管中GoldenGroup高地集团澳大利亚| 5-10年85.87
- 监管中IC Markets10-15年 | 澳大利亚监管 | 塞浦路斯监管91.71
- 监管中CPT Markets Limited5-10年 | 英国监管 | 伯利兹监管91.56
- 监管中AUS Global5-10年 | 塞浦路斯监管 | 澳大利亚监管86.47
- 监管中OneRoyal10-15年 | 澳大利亚监管 | 塞浦路斯监管 | 瓦努阿图监管85.75
- 监管中易信easyMarkets15-20年 |澳大利亚监管 | 塞浦路斯监管85.38
- 监管中FXCC10-15年 | 塞浦路斯监管 | 直通牌照(STP)85.26