创新药大事件 | 抗癌多面手,君实生物特瑞普利单抗杀疯了!一个月内两项Ⅲ期临床达到主要终点
PD-1/PD-L1是国内创新药研发领域大热的赛道,恒瑞、君实、百济等国产创新药龙头企业针对该领域均有诸多布局。截至2022年12月,国内市场已上市15款PD-1/PD-L1药物。对于PD-1/PD-L1药物而言,以小适应获批上市,逐步拓展更多适应症是普遍采取的发展策略。
而作为我国首个批准上市的以PD-1为靶点的国产单抗药物,君实生物的特瑞普利单抗近期以来在适应症拓展方面获得了诸多重大突破。2月20日,君实生物发布公告称特瑞普利单抗联合化疗用于晚期三阴性乳腺癌患者治疗的III期临床研究达到主要研究终点。
值得一提的是,仅一个月前,特瑞普利单抗联合化疗用于可手术非小细胞肺癌患者围手术期治疗的III期临床研究达到主要研究终点。一个月内,两个适应症的Ⅲ期临床达到主要终点,这在PD-1/PD-L1药物中可谓是前所未有独一份。那么,特瑞普利单抗究竟有多“能打”,其未来市场价值又有几何呢?
荣誉满身的抗癌多面手——特瑞普利单抗
特瑞普利单抗是中国首个批准上市的以PD-1为靶点的国产单抗药物,曾荣膺国家专利领域最高奖项“中国专利金奖”,至今已在全球(包括中国、美国、东南亚及欧洲等地)开展了覆盖超过15个适应症的30多项临床研究。截至目前,特瑞普利单抗的6项适应症已于中国获批。
2020年12月,特瑞普利单抗注射液首次通过国家医保谈判,目前已有3项适应症纳入国家医保目录(2021年版)。值得关注的是,特瑞普利单抗注射液也是国家医保目录中唯一批准用于治疗黑色素瘤和鼻咽癌的抗PD-1单抗药物,并获得2019年和2020年版《中国临床肿瘤学会(CSCO)黑色素瘤诊疗指南》推荐。
此外,在海外市场,特瑞普利单抗已在黏膜黑色素瘤、鼻咽癌、软组织肉瘤、食管癌及小细胞肺癌领域获得FDA授予2项突破性疗法认定、1项快速通道认定、1项优先审评认定和5项孤儿药资格认定。
特瑞普利单抗之所以受到国内外市场的一致认可,还要从其在多项Ⅲ期临床中取得的出色临床数据说起。以君实生物最新披露的特瑞普利单抗联合化疗用于晚期三阴性乳腺癌患者治疗的III期临床研究为例。近年来,国外已有研究显示晚期三阴性乳腺癌接受免疫治疗联合化疗有较好的疗效及耐受性。
但目前中国尚无针对晚期三阴性乳腺癌的免疫治疗药物获批,治疗仍以化疗为主,可选择的药物包括蒽环类药物、紫杉烷、铂类药物等。但无论单药或是联合化疗均疗效欠佳,中位生存期约9至12个月,5年生存率不足30%。
而在特瑞普利单抗联合注射用紫杉醇用于首诊IV期或复发转移性三阴性乳腺癌患者治疗的随机、双盲、安慰剂对照、多中心III期临床研究中,据研究期中分析结果,与注射用紫杉醇相比,特瑞普利单抗联合注射用紫杉醇可显著延长PD-L1阳性人群的无进展生存期,同时,全人群和PD-L1阳性人群的次要终点——总生存期也显示出明显获益趋势。
根据上述结果,独立数据监查委员会(IDMC)判定研究的主要终点达到方案预设的优效界值。此外,特瑞普利单抗联合化疗在一线治疗非小细胞肺癌、一线治疗鼻咽癌、一线治疗晚期或转移性食管鳞癌等多项Ⅲ期临床中,均显示出良好的治疗效果。
所谓一线治疗,就是对于某个疾病使用对该病最有效,最敏感的药物。对于疾病的治疗,在药物方面有一线药和二线药,还有三、四线。通常而言没有其他并发症和禁忌症的都会选择一线药物进行治疗,因为一线药物成熟,对疾病敏感,副作用相对比较小。二三线药物是作为备选,实在不合适用一线才用二线。因此,特瑞普利单抗三项一线治疗方案均已于国内获批,也侧面说明了其出色的临床价值。
全面发力,君实业绩拐点或将到来
自2019年特瑞普利单抗上市以来,君实生物收入持续增长,一方面来自于特瑞普利销售贡献,另一方面来自于技术许可、里程碑收入等。2021年特瑞普利单抗三线后治疗鼻咽癌和二线治疗尿路上皮癌适应症纳入医保,使得其在销售收入实现较大增幅,2022年前三季度销售额达5.15亿,销售收入环比不断提升。
同时,随着更多重磅适应症,如一线治疗食管鳞癌、一线治疗非小细胞肺癌获批并进入商业化阶段,特瑞普利单抗销售额有望进一步实现大幅跃迁。
特瑞普利单抗获批上市情况
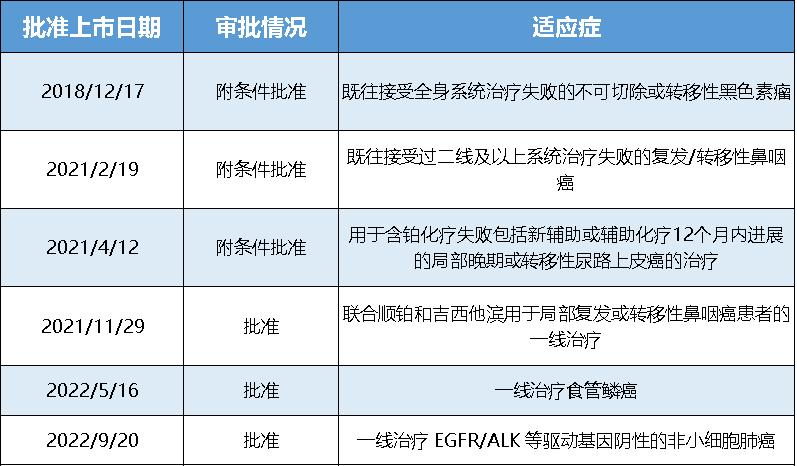
资料来源:公开信息整理 金融界上市公司研究院
以大适应症非小细胞癌为例,资料显示,肺癌是目前全球发病率第二、死亡率第一的恶性肿瘤,在中国的发病率和死亡率亦位列第一。根据世界卫生组织发布的数据,2020年中国新发肺癌病例数为81.6万,占中国新发癌症病例数的17.9%,2020年中国肺癌死亡病例数为71.5万,占中国癌症死亡病例数的23.8%。而非小细胞肺癌为肺癌的主要亚型,约占所有病例的85%。在非小细胞肺癌中非鳞状非小细胞肺癌患者占比约70%。
现有国内外研究表明,抗PD-(L)1单抗单药或联合化疗已成为一线晚期驱动基因阴性非小细胞肺癌的新标准治疗。目前国内其他获批一线治疗驱动基因阴性的非小细胞肺癌药物包括信达生物的信迪利单抗、恒瑞医药的卡瑞利珠单抗、百济神州的替雷利珠单抗等。而特瑞普利单抗的获批则代表其正式进入大适应症领域,将为君实生物提供新的快速增长动力。
据浙商证券测算,仅一线晚期驱动基因阴性的非小细胞肺癌这一个适应症,卡瑞利珠单抗即有望在2023年实现2.1亿元的销售额。此外,对于2022年5月获批的一线治疗食管鳞癌适应症,卡瑞利珠单抗也有望于今年实现1.32亿元的销售额。
国际化方面,根据君实生物2023年2月20日发布的公告显示,特瑞普利单抗联合顺铂和吉西他滨用于局部复发或转移性鼻咽癌患者的一线治疗、特瑞普利单抗联合紫杉醇和顺铂用于不可切除局部晚期/复发或转移性食管鳞癌患者的一线治疗的上市许可申请已获得英国药品和保健品管理局受理。
同时鼻咽癌适应症在2022年5月收到FDA回复后也已于7月份重新提交BLA,综上可以清晰的看出,凭借出色的临床药用价值,特瑞普利单抗新适应症未来出海的可能性值得期待,有望为国产创新药出海再添新丁并为君实生物带来新的业绩增长动力。
写在最后
结合2月20日两项新适应症Ⅲ期临床达到主要终点来看,特瑞普利单抗的未来还远不止于此。据公开资料显示,君实生物至今已在全球开展了覆盖超过15个适应症的30多项临床研究。
同时君实还积极推动特瑞普利单抗在肿瘤免疫治疗中“全线贯穿”的应用,目前特瑞普利单抗的围手术期或术后辅助疗法已在肺癌、食管癌、肝癌、胃癌等大癌种研究中进入III期临床阶段。由此可见,特瑞普利单抗或许将在不久的将来进入适应症收获井喷期,让我们拭目以待。
交易商排行
更多- 监管中EXNESS10-15年 | 英国监管 | 塞浦路斯监管 | 南非监管93.02
- 监管中FXTM 富拓10-15年 |塞浦路斯监管 | 英国监管 | 毛里求斯监管88.21
- 监管中FXBTG10-15年 | 澳大利亚监管 |83.48
- 监管中GoldenGroup高地集团澳大利亚| 5-10年85.87
- 监管中IC Markets10-15年 | 澳大利亚监管 | 塞浦路斯监管91.71
- 监管中CPT Markets Limited5-10年 | 英国监管 | 伯利兹监管91.56
- 监管中AUS Global5-10年 | 塞浦路斯监管 | 澳大利亚监管86.47
- 监管中OneRoyal10-15年 | 澳大利亚监管 | 塞浦路斯监管 | 瓦努阿图监管85.75
- 监管中易信easyMarkets15-20年 |澳大利亚监管 | 塞浦路斯监管85.38
- 监管中FXCC10-15年 | 塞浦路斯监管 | 直通牌照(STP)85.26


